Von der Gelenkembolisation zur Sehnenbehandlung
Die Behandlung chronischer muskuloskelettaler Schmerzen befindet sich derzeit in einem signifikanten Wandel. Während die interventionelle Radiologie traditionell auf vaskuläre Pathologien und Onkologie fokussiert war, etabliert sich mit der muskuloskelettalen Embolisation (MSK-Embolisation) ein neues therapeutisches Feld. Historisch betrachtet galten Sehnen- und Gelenkschmerzen als rein biomechanisches oder degeneratives Problem. Neuere histopathologische Erkenntnisse zeigen jedoch, dass chronische Schmerzen untrennbar mit einer pathologischen Angiogenese (Gefäßneubildung) verbunden sind (1).
Bevor die Technik auf Sehnen übertragen wurde, lieferte die Behandlung der Kniearthrose (Osteoarthritis, OA) den klinischen Beweis (“Proof of Concept”). Bei der Osteoarthritis korreliert der Schmerzgrad oft nicht direkt mit dem radiologischen Schweregrad der Arthrose, sondern vielmehr mit dem Grad der Synovitis. Diese chronische Entzündung der Gelenkinnenhaut wird durch pathologische Neovaskularisation unterhalten.
Die Embolisation der Genikulararterien (GAE) zielt darauf ab, diese hyperämischen Areale selektiv zu devaskularisieren. In einer wegweisenden prospektiven Multicenter-Studie zeigten Bagla et al., dass die GAE den WOMAC-Score signifikant verbessert (2). Landers et al. bestätigten in einer systematischen Übersichtsarbeit, dass die GAE eine sichere und effektive Methode zur Reduktion von OA-bedingten Schmerzen ist, mit einer Erfolgsrate von über 80 % in der kurz- bis mittelfristigen Beobachtung (3). Aktuelle Daten unterstreichen zudem die Langlebigkeit der Ergebnisse, wobei viele Patienten auch 1–2 Jahre post-interventionell eine klinisch relevante Schmerzreduktion aufweisen (4).
Dieser Erfolg am Kniegelenk führte zur Hypothese, dass ähnliche pathophysiologische Mechanismen – nämlich die Koppelung von Neovaskularisation und Schmerz – auch bei extraartikulären Pathologien wie Tendinopathien vorliegen. Dies war die Geburtsstunde der TAME (Transarterielle Mikroembolisation) bei Tendinopathien.
Pathophysiologie: Das neurovaskuläre Modell
Das Verständnis der TAME basiert auf dem Konzept des “Angio-Neuralen Cross-Talks”. Physiologische Sehnen sind bradytroph und weiß glänzend. Bei chronischen Tendinopathien zeigt sich makroskopisch und histologisch jedoch eine deutliche Hypervaskularisation.
Neovaskularisation: Durch repetitive Mikrotraumata und fehlgeschlagene Reparaturprozesse sprießen Kapillaren aus dem umliegenden Gewebe in die Sehne ein. Diese Gefäße sind dysfunktional; ihnen fehlt eine reguläre Tunica media (glatte Muskulatur), weshalb sie permanent dilatiert sind.
Neoinervation: Wichtiger für die Schmerzentstehung ist, dass Blutgefäße und Nerven gemeinsam wachsen. Alfredson et al. wiesen nach, dass diese Neogefäße von sensorischen Nervenfasern (C-Fasern) begleitet werden, die Substanz P und Calcitonin Gene-Related Peptide (CGRP) exprimieren (5).
Der Teufelskreis: Die Nervenfasern sind für den Ruheschmerz und Druckschmerz verantwortlich. Gleichzeitig unterhalten die Gefäße durch den Einstrom von Entzündungsmediatoren die Chronifizierung. Die TAME unterbricht diesen Kreislauf mechanisch und chemisch, indem sie den Blutfluss in den pathologischen Gefäßen stoppt, was zur Ischämie der Nervenenden und zur Rückbildung der Entzündung führt (6).
Fokus: Plantarfasziitis
Die Plantarfasziitis ist eine der häufigsten Ursachen für Fersenschmerzen und betrifft etwa 10 % der Bevölkerung im Laufe ihres Lebens. Obwohl oft als “Entzündung” bezeichnet, handelt es sich primär um einen degenerativen Prozess der Plantarfaszie am Ursprung des Calcaneus.
Rationale für die Embolisation: Bei etwa 10 % der Patienten entwickelt sich eine chronische, therapierefraktäre Verlaufsform. Hochauflösende Ultraschalluntersuchungen (Power-Doppler) zeigen bei diesen Patienten fast immer eine ausgeprägte Hyperämie am medialen Calcaneus-Tuberkel. Dies macht die Plantarfasziitis zu einem idealen Zielgebiet für die TAME.
Evidenzlage zur Plantarfasziitis: Die Ergebnisse der TAME bei Plantarfasziitis sind in der Literatur hervorragend dokumentiert. Okuno et al. behandelten in einer Studie 59 Patienten mit therapierefraktärer Plantarfasziitis. Der mittlere VAS-Score sank von 7,3 vor der Behandlung auf 2,7 nach 6 Monaten. Nach 2 Jahren lag der Wert bei 0,9. Es wurden keine schwerwiegenden Komplikationen beobachtet (7).
Eine neuere Untersuchung von Hwang et al. bestätigte diese Daten im Langzeitverlauf. In ihrer Kohorte berichteten 85 % der Patienten über eine signifikante Verbesserung der Lebensqualität und Wiedererlangung der Gehfähigkeit ohne Einschränkung (8).
Zudem deutet eine vergleichende Analyse von Kim et al. darauf hin, dass die Embolisation bei Patienten, die auf Stoßwellentherapie (ESWT) nicht ansprachen, als effektive “Salvage-Therapie” dient (9).
Fokus: Achillessehnentendinitis
Neben der Plantarfasziitis stellt die chronische Achillessehnentendinitis eine der größten Herausforderungen in der Sportmedizin dar. Besonders die sogenannte “Mid-portion”-Tendinopathie ist oft resistent gegenüber konservativen Maßnahmen.
Pathologische Besonderheit: Ähnlich wie bei der Plantarfaszie korreliert der Schmerz bei der Achillessehnentendinitis stark mit dem Einsprießen von Neogefäßen aus dem Kager-Fettkörper (ventral) in die Sehne. Diese Areale sind im Doppler-Ultraschall gut darstellbar.
Klinische Evidenz: Die TAME bietet hier einen entscheidenden Vorteil, da sie das bei Kortisoninjektionen gefürchtete Risiko einer Sehnenruptur vermeidet. Aktuelle, vielversprechende Ergebnisse wurden kürzlich von Homs et al. publiziert. In ihrer Studie zur Behandlung der therapieresistenten Achillessehnentendinitis mittels TAME konnte eine signifikante Reduktion des VAS-Schmerzscores beobachtet werden. Die Intervention erwies sich als technisch machbar und sicher, ohne negative Auswirkungen auf die Sehnenstruktur (10).
Auch Okuno et al. zeigten bereits in früheren Kohorten, dass die Embolisation bei Achillessehnenbeschwerden effektiv ist, wobei die klinische Verbesserung oft der morphologischen Verbesserung im MRT vorausgeht (1). Dies ist besonders für Leistungssportler relevant, da die TAME keine Ruhigstellung erfordert und ein schnelleres “Return-to-Play” ermöglichen kann als chirurgische Debridements.
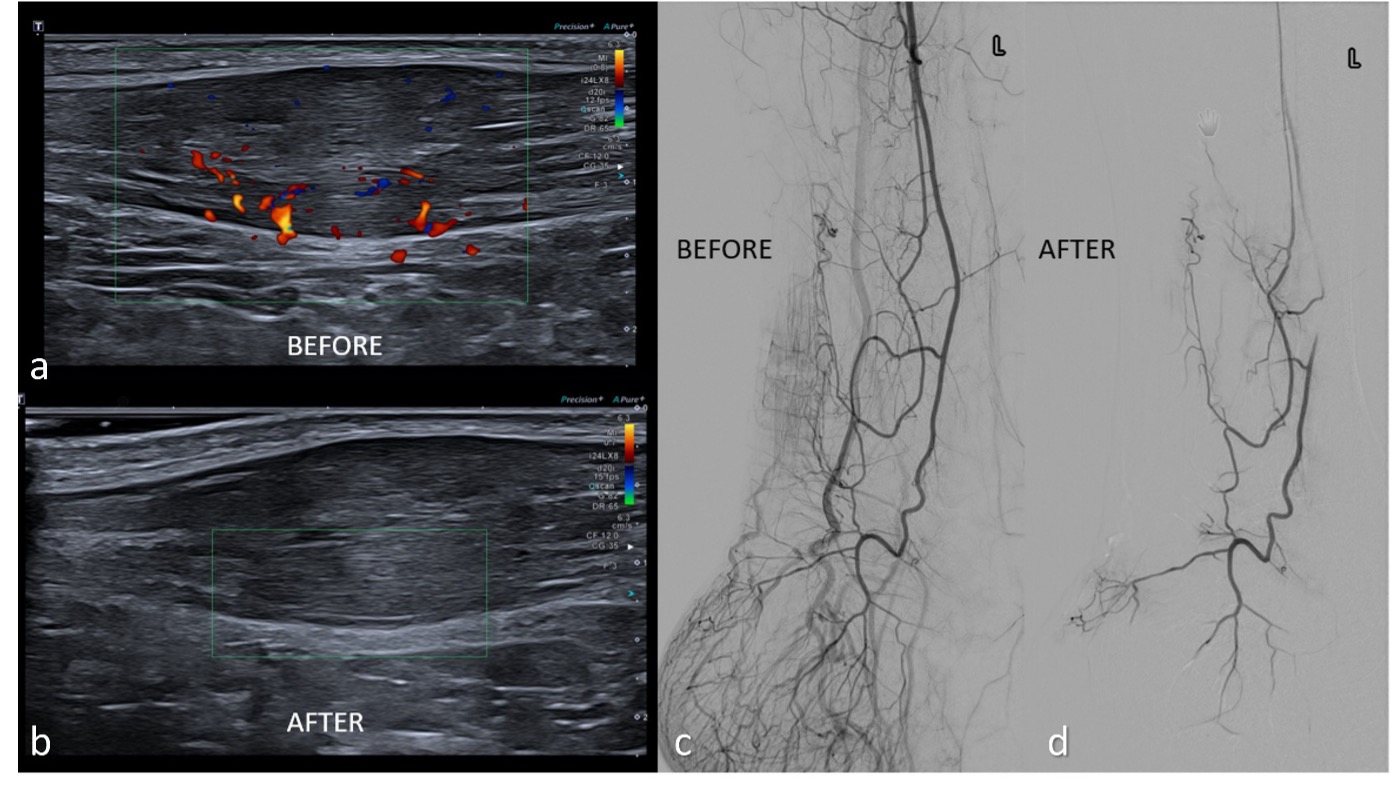
Abb. 1: a. Duplex-sonographische Darstellung der deutlich aufgetriebenen Achillessehne im mittleren Drittel (Mid-Portion – Tendinitis) mit vermehrter Vaskularisation im ventralen Aspekt vor TAME. Korrespondierend digitale Subtraktionsangiographie (DSA) nach selektiver Sondierung der Arteria fibularis mit Darstellung der deutlichen Hyperämie der Achillessehne (c). Postembolisation Duplex-Ultraschall (b) und DSA (d) nach TAME mit Abbildung einer nahezu vollständigen Drosselung der Achillessehnen-Hyperämie.
Methodik und Materialien: Warum temporäre Embolisation?
Ein Schlüsselelement der TAME bei Tendinopathien ist die Wahl des Embolisationsmaterials. Im Gegensatz zur Tumortherapie wird hier meist eine Mischung aus Imipenem/Cilastatin verwendet.
Wirkmechanismus: Imipenem bildet in Suspension mit NaCL oder Kontrastmittel schwerlösliche Mikropartikel (ca. 10–70 μm). Diese verstopfen die Kapillaren. Da Imipenem im Blut löslich ist, rekanalisieren sich die Gefäße nach ca. 1-2 Stunden. Diese Zeitspanne reicht aus, um die fragilen Neogefäße (ohne Muskelschicht) nekrotisieren zu lassen (Hypoxie-Sensitivität), während die gesunden Gefäße und das Hautgewebe (die robustere Kollateralen besitzen) die kurzzeitige Ischämie unbeschadet überstehen (6). Die Nutzung permanenter Partikel (z.B. PVA) in oberflächlichen Arealen birgt ein Risiko für Hautnekrosen. Die temporäre Embolisation eliminiert dieses Risiko nahezu vollständig.
Weitere Anwendungsgebiete
Die TAME hat sich über Fuß und Sprunggelenk hinaus bei weiteren Entitäten als wirksam erwiesen:
Epicondylitis humeri (Tennis-/Golferellenbogen): Die laterale Epicondylitis zeigt exzellente Ansprechraten. Okuno et al. berichteten in ihrer ersten Kohorte von einer Schmerzreduktion von VAS 7,3 auf 1,8 nach 2 Jahren. Die Griffkraft blieb erhalten (1).
Adhesive Capsulitis (Frozen Shoulder): Hier zielt die Embolisation auf die Neovaskularisation im Rotatorenintervall. Fernández-López et al. zeigten in einem Review, dass die Embolisation zu einer schnelleren Wiederherstellung der Range of Motion (ROM) führt als rein konservative Therapie (11).
Patellaspitzensyndrom (Jumper’s Knee): Hier ist die Embolisation besonders wertvoll, da Kortisoninjektionen wegen der Rupturgefahr der Patellasehne kontraindiziert sind.
Vergleich zu konservativen Maßnahmen
Die Einordnung der TAME in den klinischen Algorithmus erfordert den Vergleich mit Standardtherapien:
Exzentrisches Training: Der Goldstandard für Sehnenpathologien. Es fördert den Kollagenumbau. Allerdings zeigt sich eine Versagerquote von 20–30 %, und die Therapie erfordert hohe Compliance über Monate (5).
Kortikosteroide: Bieten schnelle, kurzfristige Linderung, wirken aber katabol. Coombes et al. zeigten in einem Review, dass Kortison das langfristige Ergebnis verschlechtern kann und das Risiko für Sehnenrupturen erhöht (12). Bei der Plantarfasziitis besteht zudem die Gefahr der Fettpolsteratrophie, was zu chronischen Belastungsschmerzen führt (13).
Stoßwellentherapie (ESWT): Eine gute nicht-invasive Option. Studien zeigen jedoch Grenzen bei chronifizierten Verläufen auf, wo die ESWT nicht immer effektiv ist (14).
PRP (Platelet-Rich Plasma): Zielt auf Regeneration ab. Die Studienlage ist heterogen; Tsikopoulos et al. fanden bei Plantarfasziitis gemischte Evidenz bezüglich der Überlegenheit gegenüber Placebo oder anderen Injektionen (15).
Fazit zum Vergleich: TAME ist indiziert, wenn mechanische (Training/Stoßwelle) und regenerative Ansätze (PRP) versagt haben, bietet aber gegenüber Kortison den entscheidenden Vorteil der Strukturschonung.
Dochu: Die Alternative zur klassischen transarteriellen Punktion
Dochu (kurz für Doumyaku-Chuusha, japanisch für „arterielle Injektion“) gilt als vereinfachtes Verfahren zur Behandlung oberflächlicher Sehnenveränderungen. Mit modernen Hochfrequenz-Ultraschallgeräten lassen sich die feinen versorgenden Arterien („Feeding Arteries“), die oft nur einen Durchmesser von 0,5 bis 1 mm aufweisen, direkt identifizieren. Durch eine Direktpunktion des zuführenden Gefäßes werden resorbierbare Mikropartikel (Imipenem/Cilastatin) unter permanenter Ultraschallkontrolle intraarteriell injiziert (16).
Die wesentlichen Vorteile liegen in der fehlenden Strahlenbelastung, der schnellen Durchführbarkeit (ca. 5–10 Minuten) und dem gesteigerten Patientenkomfort, da auf das Einführen eines Katheters verzichtet wird. Das Verfahren erfordert jedoch ein hohes Maß an sonographischem Geschick und manueller Präzision: Da das Zielgefäß winzig ist, muss das Embolisat exakt intraarteriell appliziert werden, um eine Injektion in das umliegende Gewebe zu vermeiden.
Dochu wird als pragmatische Weiterentwicklung für spezifische Indikationen betrachtet: Während komplexe Befunde (wie ausgeprägte Schultersteife oder Kniearthrose) oft weiterhin die angiographische Übersicht der klassischen TAME erfordern, stellt Dochu für gut zugängliche Sehnenansätze eine effektive und weniger invasive Alternative dar (17, 18).
Literaturverzeichnis
(1) Okuno Y, et al. (2013). Transcatheter arterial embolization using imipenem/cilastatin sodium for tendinopathy and enthesopathy refractory to non-surgical management. Journal of Vascular and Interventional Radiology, 24(6), 787-792.
(2) Bagla S, et al. (2020). Genicular Artery Embolization for the Treatment of Knee Pain Secondary to Osteoarthritis. Journal of Vascular and Interventional Radiology, 31(7), 1096-1102.
(3) Landers S, et al. (2022). Genicular Artery Embolization for Osteoarthritis Related Knee Pain: A Systematic Review and Meta-analysis. CardioVascular and Interventional Radiology.
(4) Little MW, et al. (2021). Genicular artery embolization in patients with osteoarthritis of the knee (GENESIS) using permanent microspheres: Interim analysis. CardioVascular and Interventional Radiology.
(5) Alfredson H, et al. (2003). Glutamate NMDAR1 receptors localised to nerves in human Achilles tendons. Clinical Orthopaedics and Related Research, 400: 165-173.
(6) Okuno Y. (2017). Interventional Management of Musculoskeletal Pain. CardioVascular and Interventional Radiology.
(7) Okuno Y, et al. (2016). Clinical Outcomes of Transcatheter Arterial Embolization for Resistant Plantar Fasciitis. Journal of Vascular and Interventional Radiology, 27(8), 1195-1202.
(8) Hwang JH, et al. (2023). Long-term Outcomes of Transcatheter Arterial Embolization for Plantar Fasciitis Refractory to Conservative Treatment. Journal of Vascular and Interventional Radiology.
(9) Kim DH, et al. (2021). Comparative study of ESWT vs. Embolization in recalcitrant plantar fasciitis. Pain Medicine.
(10) Homs J, et al. (2024). Transarterial periarticular embolization (TAPE) for treatment of achillodynia: initial results. RöFo – Fortschritte auf dem Gebiet der Röntgenstrahlen.
(11) Fernández-López X, et al. (2022). Embolization of the shoulder for adhesive capsulitis: A systematic review. Diagnostic and Interventional Imaging, 103(12), 701-707.
(12) Coombes BK, Bisset L, Vicenzino B. (2010). Efficacy and safety of corticosteroid injections and other injections for management of tendinopathy: a systematic review of randomised controlled trials. The Lancet, 376(9754), 1751-1767.
(13) Tatli YZ, Kapasi S. (2012). The real risks of steroid injection for plantar fasciitis, with a review of the literature. Current Reviews in Musculoskeletal Medicine.
(14) Mani-Babu S, et al. (2015). The effectiveness of extracorporeal shock wave therapy in lower limb tendinopathy: a systematic review. American Journal of Sports Medicine.
(15) Tsikopoulos K, et al. (2016). Injection therapies for plantar fasciopathy (‘plantar fasciitis’): a systematic review and network meta-analysis of 22 randomised controlled trials. British Journal of Sports Medicine.
(16) Sasaki T, et al. (2025). Clinical results of ultrasound-guided intra-arterial embolization targeting abnormal neovessels for plantar fasciitis: 66 cases with up to 4 years of follow-up.
(17) Kubo T, et al. (2023). Intra-Arterial Injection of Temporary Embolic Material Through a Needle Inserted into the Radial or Ulnar Artery for Distal and Proximal Interphalangeal Joint Osteoarthritis: A Retrospective Study of 92 Patients.
(18) Inui S, et al. (2021). Intra-arterial infusion of Imipenem/Cilastatin sodium through a needle inserted into the radial artery as a new treatment for refractory Trapeziometacarpal osteoarthritis.
Priv.-Doz. Dr. Alexander Loizides CV
 Priv.-Doz. Dr. Alexander Loizides ist Assistenzprofessor für Radiologie und stellvertretender Leiter der Abteilung für endovaskuläre und interventionelle Radiologie an der Universitätsklinik für Radiologie der Medizinischen Universität Innsbruck. Dort schloss er seine Facharztausbildung mit einem klaren Fokus auf die muskuloskelettale und interventionelle Radiologie ab und habilitierte sich zum Thema der peripheren Nervensonographie. Als anerkannter Experte auf seinem Gebiet ist Dr. Loizides Autor und Koautor zahlreicher Publikationen in internationalen Fachzeitschriften sowie mehrerer Fachbücher; unter anderem fungiert er als Herausgeber der Werke „Nerve Sonography“ (2018), „Sonographic Peripheral Nerve Topography“ (2019) und „Ultrasound-guided Musculoskeletal Embolotherapies using the „Dochu“ Technique“ (2026). Neben seiner Tätigkeit als Reviewer für verschiedene wissenschaftliche Journale engagiert er sich in führenden Fachgesellschaften wie der Österreichischen Röntgengesellschaft (ÖRG), der Österreichischen Gesellschaft für Interventionelle Radiologie & minimal-invasive Therapie (ÖGIR) sowie der Österreichischen Gesellschaft für Ultraschall in der Medizin (ÖGUM). Seine Leidenschaft für die interventionelle Radiologie und sein spezieller Fokus auf die muskuloskelettale Bildgebung und Schmerztherapie führten ihn zur Gründung des Vereins „DISI – Verein zur Förderung sonographischer Wissensgewinnung“. Gemeinsam mit seinen Kollegen organisiert Dr. Loizides regelmäßig Workshops und hält Vorträge auf nationalen und internationalen Kongressen um die Qualität minimal-invasiver Behandlungen stetig zu verbessern und die Grenzen der interventionellen Radiologie in neue diagnostische Felder zu verschieben.
Priv.-Doz. Dr. Alexander Loizides ist Assistenzprofessor für Radiologie und stellvertretender Leiter der Abteilung für endovaskuläre und interventionelle Radiologie an der Universitätsklinik für Radiologie der Medizinischen Universität Innsbruck. Dort schloss er seine Facharztausbildung mit einem klaren Fokus auf die muskuloskelettale und interventionelle Radiologie ab und habilitierte sich zum Thema der peripheren Nervensonographie. Als anerkannter Experte auf seinem Gebiet ist Dr. Loizides Autor und Koautor zahlreicher Publikationen in internationalen Fachzeitschriften sowie mehrerer Fachbücher; unter anderem fungiert er als Herausgeber der Werke „Nerve Sonography“ (2018), „Sonographic Peripheral Nerve Topography“ (2019) und „Ultrasound-guided Musculoskeletal Embolotherapies using the „Dochu“ Technique“ (2026). Neben seiner Tätigkeit als Reviewer für verschiedene wissenschaftliche Journale engagiert er sich in führenden Fachgesellschaften wie der Österreichischen Röntgengesellschaft (ÖRG), der Österreichischen Gesellschaft für Interventionelle Radiologie & minimal-invasive Therapie (ÖGIR) sowie der Österreichischen Gesellschaft für Ultraschall in der Medizin (ÖGUM). Seine Leidenschaft für die interventionelle Radiologie und sein spezieller Fokus auf die muskuloskelettale Bildgebung und Schmerztherapie führten ihn zur Gründung des Vereins „DISI – Verein zur Förderung sonographischer Wissensgewinnung“. Gemeinsam mit seinen Kollegen organisiert Dr. Loizides regelmäßig Workshops und hält Vorträge auf nationalen und internationalen Kongressen um die Qualität minimal-invasiver Behandlungen stetig zu verbessern und die Grenzen der interventionellen Radiologie in neue diagnostische Felder zu verschieben.

